ALBU external quality assessment analysiscombined with experiment of performance verification
-
摘要:
目的通过检测系统性能验证,分析尿白蛋白室间质评成绩不满意的可能原因及是否影响临床样本检测。 方法回顾室内质控结果,检查仪器及试剂状态;复检剩余的EQA质控样本;对于透散比浊法、散射比浊法检测尿白蛋白进行分析测量范围验证(EP6-A);检测40份患者尿液样本,对于透射比浊法、散射比浊法检测准确度差异进行分析(EP9-A2);分析CAP尿液能力验证实验结果,与其他实验室进行临床样本比对。结果室内质控均在控,复测结果与上报结果一致,分析测量范围分析显示两个方法没有显著差异,两种方法检测患者新鲜尿标本差异在允许误差范围内;两次CAP质评回报满意(PT=100%),两种方法间无明显差异;与其他实验室两次比对偏奇在1/2PT范围内。 结论本实验室透散比浊法、散射比浊法检测尿白蛋白尿白差异小,准确度好,室间质评成绩不影响临床样本的检测质量。 Abstract:Objective To analyse the reasons of ALBU EQA unacceptable. Methods The quality control data were reviewed, the EQC samples stored in -80 ℃ were reran with instruction status checked. Measuring range evaluation of ALBU of turbidimetry and scatteringmetry were performed. The accuracy of turbidimetry and scatteringmetry were ompareed through detected ALBU in 40 clinical samples. ALBU CAP proficiency testing results were analyzed. Results The IQC data were in control, rerun data were accordance with reported data, the ALBU measuring range of turbidimetry and scatteringmetry is uniformity, the accuracy of turbidimetry and scatteringmetry detecting ALBU in clinical samples were similar. The evaluation results of CAP proficiency testing were acceptable, the bias between turbidimetry and scatteringmetry detecting ALBU were limited. Conclusion ALBU EQC unacceptable will not affect the accuracy of clinical sample results . -
Key words:
- EQC /
- performance verification /
- CAP /
- PT
-
表 1 两次国内室间质评结果(mg/L)
第1 次EQC 我室结果(透射比浊法) 允许范围 评价结果(PT:0%) 第2 次EQC 我室结果(散射比浊法) 允许范围 评价结果(PT:40%) 1 28.4 9.94~18.46 未通过 1 17.6 19.56~36.34 未通过 2 92.3 42.49~78.91 未通过 2 67.3 47.11~87.49 通过 3 95.4 42.42~78.78 未通过 3 19.8 22.43~41.66 未通过 4 39.2 10.15~18.85 未通过 4 61.9 44.10~81.90 通过 5 119.2 51.94~96.46 未通过 5 18.4 21.88~40.62 未通过 表 2 散射比浊与透射比浊法复测质控物结果(mg/L)
第1 次QC 允许范围 散射比浊法 透射比浊法 原结果 复检结果 复检评价 原结果 复检结果 复检评价 1 9.94~18.46 - 12 通过 28.4 32.43 未通过 2 42.49~78.91 - 53.5 通过 92.3 108.95 未通过 3 42.42~78.78 - 53.6 通过 95.4 113.28 未通过 4 10.15~18.85 - 12.7 通过 39.2 47.59 未通过 5 51.94~96.46 - 64.9 通过 119.2 149.96 未通过 第2 次QC 允许范围 散射比浊法 透射比浊法 原结果 复检结果 复检评价 原结果 复检结果 复检评价 1 19.56~36.34 17.6 14.9 未通过 - 32.52 通过 2 47.11~87.49 67.3 61.7 通过 - 96.25 未通过 3 22.43~41.66 19.8 15.7 未通过 - 33.05 通过 4 44.1~81.9 61.9 55.3 通过 - 90.08 未通过 5 21.88~40.62 18.4 15.7 未通过 - 32.52 通过 表 3 分析灵敏度计算(mg/L)
检测结果 1 2 3 4 5 理论值 1.13 2.27 2.56 4.83 9.82 平均值 2.09 2.39 3.25 4.78 9.42 透射比浊法 S 0.158 0.356 0.15 0.252 0.268 CV% 7.55 14.905 4.615 5.276 2.841 平均值 2 2.027 2.358 4.564 9.068 散射比浊法 S 0 0.081 0.14 0.212 0.319 CV% 0 3.996 5.921 4.649 3.519 表 4 透射比浊法线性范围验证(全自动生化分析仪)(mg/L)
样本配制 标本编号 测量值1 测量值2 均值 8L 1 1.6 1.24 1.42 7L+H 2 32.8 32.21 32.51 6L+2H 3 67.4 68.02 67.71 5L+3H 4 102.2 99.82 101.01 4L+4H 5 136.4 129.46 132.93 3L+5H 6 171.4 166.1 168.75 2L+6H 7 207.1 201.14 204.12 L+7H 8 242.5 232.95 237.73 8H 9 277.7 277.1 277.4 多项式回归 1st b1 34.336 t(v=16) 113.008 2nd b2 0.302 t(v=15) 3.991 3rd b2 -0.256 -0.485 3rd b3 0.037 t(v=14) 1.069 符合二元二次方程 测量均值 预期值1st 预期值2nd 差值(2nd-1st) % 差值 1.42 1.32 1.43 0.117 0.089 32.505 32.95 33.65 0.704 0.0214 67.71 67.28 66.47 -0.81 -0.012 101.01 101.62 99.9 -1.72 -0.0169 132.93 135.95 133.93 -2.026 -0.0149 168.75 170.29 168.56 -1.728 -0.0101 204.12 204.63 203.8 -0.826 -0.004 237.725 238.96 239.64 0.68 0.0028 277.4 273.3 276.09 2.79 0.0102 *9个浓度点偏倚均在15%范围内. 表 5 散射比浊法线性范围验证(特殊蛋白分析仪)(mg/L)
样本配制 标本编号 测量值1 测量值2 均值 8L 1 2 2 2 7L+H 2 34.5 34 34.25 6L+2H 3 66.5 64 65.25 5L+3H 4 98.4 96 97.2 4L+4H 5 132 132 132 3L+5H 6 175 173 174 2L+6H 7 220 193 206.5 L+7H 8 230 217 223.5 8H 9 256 237 246.5 多项式回归 1st b1 31.751 t(v=16) 31.513 2nd b2 -0.717 t(v=15) -1.881 3rd b2 4.703 2.891 3rd b3 -0.361 t(v=14) -3.366 符合二元三次方程 测量均值 预期值1st 预期值3rd 差值(3rd-1st) % 差值 2 4.24 3.62 -0.62 -0.1457 34.25 35.99 31.29 -4.703 -0.1307 65.25 67.74 64.03 -3.714 -0.0548 97.2 99.49 99.68 0.183 0.0018 132 131.25 136.07 4.822 0.0367 174 163 171.03 8.037 0.0493 206.5 194.75 202.41 7.662 0.0393 223.5 226.5 228.03 1.531 0.0068 246.5 258.25 245.73 -12.522 -0.0485 *9个浓度点偏倚均在15%范围内. 表 6 透射比浊法/散射比浊法检测临床样本的估计误差
项目 a b r 回归方程 SE(mg/24 h 尿) 卫计委临检中心1/2PT MA -3.35 1.08 0.996 Y=1.08X-3.35 X=30 X=300 15% 1.01 20.08 0.0336 0.0669 表 7 透射比浊法、散射比浊法CAP质评结果分析(mg/L)
组别 第1 次CAP质评 第2次CAP质评 散射比浊法 透射比浊法 回报范围 散射比浊法 透射比浊法 回报范围 1 996 1003 740.9-1376.1 14.7 14.6 9.7-18.2 2 23.4 23 17.5-32.6 25.7 25 17.6-32.8 3 9.21 9.6 7-13.2 102 83.5 64.3-119.6 表 8 与其它实验室进行临床样本检测比对(散射比浊法)(mg/L)
样本编号 第1 次 第2 次 其它实验室 本室 相对偏倚(%) 其它实验室 本室 相对偏倚(%) 1 68.5 72.9 -6.04 17.2 18.1 -4.97 2 1930 1710 12.87 324 322 0.62 3 2 2 0 22.8 23 -0.87 4 7.5 7.45 0.67 826 790 4.56 5 9.34 9.13 2.3 2.52 2.42 4.13 6 903 895 0.89 7 688 635 8.35 8 9.54 9.39 1.6 -
[1] 张秀明, 庄俊华, 郑松柏, 等. 临床化学发光免疫法检测AFP的分析性能验证与实验方法[J]. 中华检验医学杂志, 2007, 30(11): 1293-7. http://www.cnki.com.cn/Article/CJFDTOTAL-ZHYJ200711031.htm [2] 冯仁丰. 临床检验质量管理技术基础[M]. 上海: 上海科学技术文献出版社, 2003: 100-36. [3] 杨有业, 张秀明. 临床检验方法学评价[M]. 北京: 人民卫生出版社, 2008: 118-93. [4] NCCLS, ISSN 0273-3099. Approved guideline NCCLS document EP6-A[S], 2003. [5] The National Committee fox Clinical Laboratory Standards. Method comparison and bias estimation using patient samples [Z]. Approved Guideline, 2nd ed EP9-A2, 2002. [6] 梁敏文, 邸玉玮, 戴耀宗, 等. 总蛋白室间质评成绩不满意原因分析 [J]. 中国误诊学杂志, 2011, 11(7): 1515-7. http://www.cnki.com.cn/Article/CJFDTOTAL-ZWZX201107002.htm -
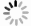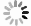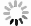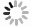






 下载:
下载: